Jelenség leírása
Mérjük meg az étolaj fajhõjét!
Eszközök
hőmérő, Kaloriméter, merülőforraló
Magyarázat
M. 139. Mérjük meg az étolaj fajhõjét!
Megoldás. Az étolaj fajhõjének megmérésére két különbözõ módszer is kínálkozik. Az elsõ, ún. ,,melegítéses módszer'' lényege a következõ:
Helyezzünk ismert mennyiségû étolajat ismert hõkapacitású, jó hõszigetelésû edénybe. Melegítsük az olajat elektromos fûtõszállal, és mérjük a leadott elektromos teljesítmény függvényében az étolaj és az edény hõmérsékletét. A kapott adatokból az olaj fajhõje meghatározható.
A második módszer a ,,keveréses módszer''. Ennél ismert mennyiségû és hõmérsékletû anyagokat hozunk egymással termikus kapcsolatba úgy, hogy közben a rendszert a környezetétõl hõszigeteléssel választjuk el. Megmérve a kialakult közös hõmérsékletet, és ismerve az egyik anyag fajhõjét, kiszámolhatjuk a másik anyag fajhõjét.
Rácz Attila (Szeged, Deák Ferenc Gimn., III. o. t.) a mérést mindkét módszerrel elvégezte. Hõszigetelt edényként mindkét esetben termoszt használt.
A melegítéses módszernél a termosz C hõkapacitásának meghatározásához elõször melegítsünk a termoszban m tömegû vizet t ideig, és mérjük a fûtõszálon átfolyó I áramot és a rajta esõ U feszültséget, valamint a melegítés hatására bekövetkezõ 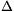 T hõmérsékletváltozást. A C hõkapacitás a következõ képlet segítségével számítható ki:
T hõmérsékletváltozást. A C hõkapacitás a következõ képlet segítségével számítható ki:
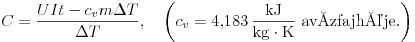
Rácz Attila 5 mérés átlagát véve a hõkapacitás értékére C = 74,8 J/K értéket kapott. Ezek után melegítsünk m tömegû olajat t ideig, és mérjük az olaj 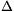 T hõmérséklet változását. Az olaj fajhõje:
T hõmérséklet változását. Az olaj fajhõje:
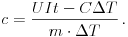
5 mérés átlagaként a fajhõre c = (1540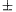 14%) J/(kg.K) adódott.
14%) J/(kg.K) adódott.
A második módszernél célszerû a termosz hõkapacitását újra meghatározni, hiszen most a fûtõszál és a vezetékek nincsenek benne a termoszban. Helyezzünk m tömegû, T1 hõmérsékletû vizet a termoszba, és öntsünk a rendszerhez m tömegû, T2 hõmérsékletû vizet. A kialakuló közös T3 hõmérséklet ismeretében a termosz hõkapacitása:
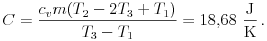
Látható, hogy ez az érték valóban különbözik a melegítéses módszernél kapott értéktõl.
Most hajtsuk végre ugyanezt a mérést, csak víz helyett használjunk étolajat. A hõmérsékletek függvényében az étolaj fajhõje:
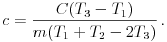
5 mérés átlagaként most az étolaj fajhõjére c = (1500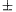 30%) J/(kg.K) adódott. Látható, hogy a két különbözõ módszerrel mért adat a mérési hibahatáron belül megegyezik.
30%) J/(kg.K) adódott. Látható, hogy a két különbözõ módszerrel mért adat a mérési hibahatáron belül megegyezik.


